|
Avertissement
|
Si vous arrivez directement
sur cette page, sachez que ce travail est un rapport d'étudiants
et doit être pris comme tel. Il peut donc comporter des
imperfections ou des imprécisions que le lecteur doit admettre
et donc supporter. Il a été réalisé pendant
la période de formation et constitue avant-tout un travail de
compilation bibliographique, d'initiation et d'analyse sur des
thématiques associées aux technologies
biomédicales. Nous ne faisons
aucun usage commercial et la duplication est libre. Si vous avez des
raisons de contester ce droit d'usage, merci de nous
en faire part . L'objectif de la présentation sur
le Web est de permettre l'accès à l'information et
d'augmenter ainsi les échanges professionnels. En cas d'usage du
document, n'oubliez pas de le citer comme source bibliographique. Bonne
lecture... |
|
MISE EN PLACE
DU GUIDE DES BONNES PRATIQUES
BIOMÉDICALES EN ÉTABLISSEMENT DE SANTÉ
|

CHTIHA HANANE
|
Référence
bibliographique à rappeler pour tout usage :
Mise en place du Guide des Bonnes Pratiques
Biomédicales en Etablissement de Santé, Hanane CHTIHA
Rapport de stage, MASTER Management des Technologies en Santé
(MTS), UTC, 2007-2008
Université de
Technologie de Compiègne
|
|
RÉSUME
Un des
objectifs de la Direction des Équipements
est l’amélioration en
continu de ses missions et ses pratiques afin de répondre au
mieux aux besoins
de ses clients, et contribuer ainsi à la sécurité
des patients. C’est pourquoi,
la Direction a pris une démarche d’implantation du Guide des
Bonnes Pratiques
Biomédicales en Établissement de
Santé, qui lui permettra à l’aide d’une grille
d’évaluation de découvrir ses
points forts et les maintenir à un niveau acceptable, mais
surtout de
concentrer ses efforts sur les points à améliorer. Une
fois que la Direction
des Équipements réalise l’auto
évaluation et met toutes les dispositions et les actions
nécessaires en œuvre
pour être conforme aux références et exigences du
guide, un examen méthodique
d’audit est réalisé afin d’évaluer la Direction
pour obtenir une validation en
« Bonnes Pratiques Biomédicales ».
Mots
clés : guide,
évaluation,
auto-évaluation, audit, validation
|
ABSTRACT
One
of the objectives of the Directorate of equipment is a continuous
improvement
of its missions and practices to address the needs of its customers,
and thus
contribute to patient safety. Therefore, the Directorate took one step
to
implement the Guide to Good Practice in Biomedical Making Health, which
will
enable it with a scoreboard to discover its strengths and to maintain a
level
acceptable, but mostly to focus on areas for improvement. Once the
Directorate
of equipment performs the self-assessment and put all measures and
actions
necessary to ensure comply with the requirements of reference and
guide,
methodical review of the audit shall be conducted to assess the
direction for a
validation in "Good Practices in Biomedical".
Keywords: guide, evaluation, self-assessment, auditing,
validation |
Je tiens
à remercier Madame Marie-Laure LOFFREDO, Directrice de
l’Hôpital
Ambroise Paré à
Boulogne-Billancourt,
pour m’avoir accueilli au sein de son établissement.
Je remercie
particulièrement Monsieur Benyounes BELHANINI, Ingénieur
Biomédical chargé de la Direction des Équipements,
pour m’avoir proposé ce
stage, pour sa disponibilité de tous les instants et pour le
suivi lors de la
conception des différentes parties du stage.
Je remercie
l’ensemble du personnel
de la Direction des Équipements pour son accueil et sa
convivialité.
Je
remercie également
Monsieur Truong Son LUU PHAN, Ingénieur Biomédical et
enseignant à l’Université
de Technologie de Compiègne, pour son aide et son soutien durant
la réalisation
de ce sujet, ainsi que Monsieur Georges CHEVALLIER, Responsable de la
spécialité Master : Management des Technologies en
Santé.
I-1)- Les consultations
spécialisées à l’hôpital
I-2)- Le plateau
médico-technique de l’hôpital
I-3)- Les moyens financiers
I-4)- Organisation de l’hôpital Ambroise Paré
II-1)- Organisation de la
Direction des Équipements
II-2)- Missions de la Direction
des Équipements
I)- Présentation
du Guide des
Bonnes Pratiques Biomédicales
I-1)- Contenu du Guide
des Bonnes Pratiques Biomédicales
I-1-1)- Bonnes Pratiques
Fonctionnelles (BPF)
I-1-2)- Bonnes
Pratiques Opérationnelles (BPO)
I-2)- Les avantages du
Guide BPB
I-3)- Pourquoi mise en place un guide
B.P.B
II)-
Présentation de la Grille
d’évaluation
II-1)- Les avantages de la
Grille d’évaluation
III)- Les
étapes d’utilisation
du guide
IV)-
Identification de la
problématique du sujet
I)- Processus de validation
II)- Les
différentes étapes de
validation en B.P.B
II-1)- Auto
évaluation
II-1-1)-
Analyse de
documentation
II-1-2)-
Grille
d’évaluation
II-1-3)-
Enquête de
satisfaction
II-1-3-1)-
Objectif de
l’enquête de satisfaction
II-1-3-2)-
Démarche mise en
œuvre
II-2)- Auto
contrôle
II-2-1)-
Réalisation d’auto
contrôle
II-2-2)- Résultat
de la 2ème auto évaluation
II-3)- Auto
déclaration
II-3-1)-
Déclaration de
conformité
II-4)-
Validation en bonnes
pratiques
retour
sommaire
La
première version du Guide des Bonnes
Pratiques Biomédicales en Établissement
de Santé est disponible gratuitement sur Internet [1],
il a été publié en
novembre 2002, sous la responsabilité de M. Gilbert Farges et
des présidents de
l'A.F.I.B., l'A.A.M.B., l'A.T.D. avec l’aide des étudiants du
D.E.S.S.
« Technologies Biomédicales
Hospitalières » de l’U.T.C., ainsi que de
nombreux acteurs biomédicaux. Ce premier
référentiel métier de la profession
biomédicale hospitalière est de plus exploité sur
le terrain. Son objectif est
de souligner le savoir-faire et le professionnalisme d'un métier
face à un
contexte réglementaire rigoureux et évolutif. Il est
considéré comme un support
crédible qui permet de justifier les moyens nécessaires
au bon fonctionnement
de tout service biomédical afin de remplir ses missions
fondamentales.
Ce Guide se
présente comme un outil stratégique de support à
une démarche
qualité et une introduction d’un cycle d'amélioration
continue, il garantit
ainsi la satisfaction du client (les services de soins et plus
particulièrement
d’une façon indirecte le patient) et assure une dynamique de
progrès.
Il
bénéficie depuis Février 2004 d’un
outil d’auto-diagnostic d’usage simple [2]. Cet outil
permet de situer en un
coup d’œil sur « une cartographie radar »
pour évaluer et
valider les « bonnes pratiques » qui peut donc
être une façon de
valoriser ses pratiques.
L’objectif de
ce sujet
est de mettre en place ce guide au sein de la Direction des Équipements
de l’hôpital Ambroise Paré à Boulogne-Billancourt
pour améliorer et remplir
correctement leurs
pratiques professionnelles et introduire un cycle d’amélioration
continue pour
satisfaire les services médicaux, médico-techniques,
administratifs et
logistiques de cet hôpital. Cette démarche qualité
sera une première étape d’un
projet de certification ISO 9001 de la
maintenance et l’achat au sein de la Direction des Équipements.
Trois grandes
parties
composent ce rapport :
- Présentation
de l’Hôpital Ambroise Paré,
- Présentation
du Guide des Bonnes Pratiques
Biomédicales en Etablissements de Santé,
- Mise
en place
des
Bonnes Pratiques Biomédicales au sein de la
Direction des Equipements.
retour sommaire
|
Chapitre I
Présentation
de l´hôpital Ambroise Paré |
I)- Présentation de
l´hôpital
L’hôpital
Ambroise Paré est un établissement de court
séjour de l’Assistance Publique - Hôpitaux de Paris
(AP-HP). Il est situé aux
portes de Paris à Boulogne-Billancourt.
C’est un centre hospitalier universitaire
médico-chirurgical de 495 lits
et places, il est le 1ercentre
d’accueil des urgences des Hauts de Seine, il dessert un secteur
sanitaire de 800 000 habitants [3].

Figure1 : Une vue
de face de l’hôpital Ambroise Paré.
La
spécialisation de l’établissement s’organise autour
de quatre grands pôles de compétence :
- le
pôle
urgences/proximité
Urgences
médico-chirurgicales adultes, neurologie et
psychiatrie de liaison, stomatologie et ORL, ophtalmologie,
médecine interne,
néphrologie, pédiatrie/secteur adolescents et urgences
enfants, chirurgie
orthopédique et traumatologie, réanimations,
gériatrie aiguë, rhumatologie.
- le
pôle
spécialités et cancérologie
Chirurgie
digestive et oncologique,
hépato-gastro-entérologie et oncologie, soins palliatifs,
dermatologie,
pneumologie, endocrinologie.
- le
pôle
radio-cardio-vasculaire
Cardiologie
et maladies vasculaires, chirurgie
vasculaire, radiologie interventionnelle, Centre de
référence national de
Marfan.
- le
pôle biologie, pathologies et produits de santé
Biochimie-hormonologie
et génétique moléculaire,
anatomie pathologique, hématologie et immunologie, microbiologie
et hygiène,
pharmacie à usage intérieur.
Nombre
de lits et places de jour autorisés
- Médecine
: 321 lits et
21 places de jour,
- Chirurgie : 147 lits et 6
places de jour,
- Total : 468 lits et
27 places de jour.
L’activité
clinique de l’hôpital
(statistique 2007)
- 160 000 personnes
accueillies en consultations externes dont 57
000 passages aux urgences adultes et enfants (soit 150 par
jour),
- 32
110 malades hospitalisés
dont 13 500 séances d’hôpital de jour,
- Durée
moyenne de séjour
: 6,1 jours,
- Taux
d’occupation : 83 %.
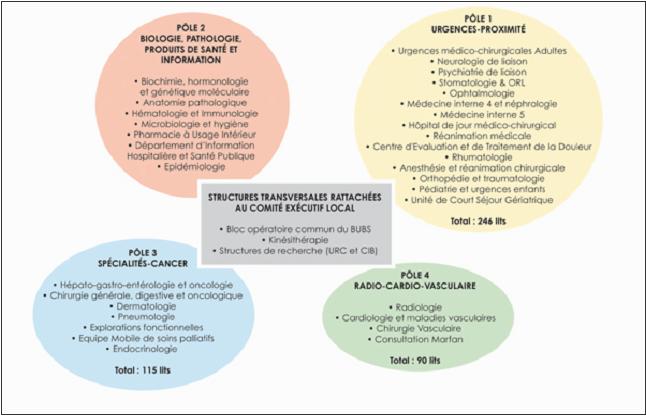
Figure 2 : la
structuration de
l’hôpital Ambroise Paré
en pôles d’activités.
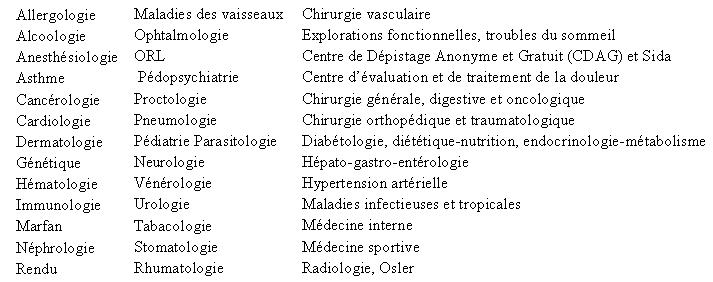
I-1)-
Les consultations spécialisées à l’hôpital
I-2)-
Le plateau medico-technique de l’hôpital
Le plateau
medico-technique est composé de : 1 bloc opératoire de 9
salles
d’opération, 1 salle de surveillance post-interventionnelle de
15 places, 11
salles de radiologie (imagerie conventionnelle, interventionnelle
vasculaire,
échographie), 1 scanner, 1 IRM et 5 laboratoires (anatomie et
cytologie
pathologiques, biochimie, biologie moléculaire et
génétique,
hématologie-immunologie, dépôt de sang
médicalisé, microbiologie et
explorations fonctionnelles).
Tableau 1:
L’activité du plateau médico-technique de
l’hôpital.
I-3)-
Les moyens financiers
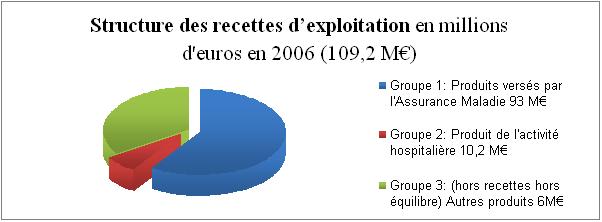
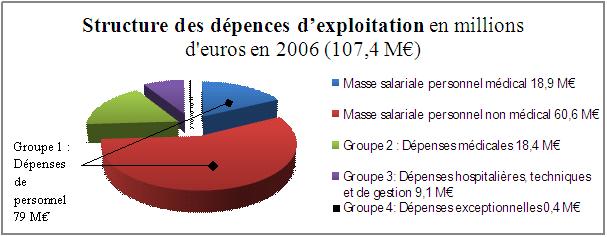
Figure
3 :
Représentation graphique du budget
d’exploitation en millions d’euros en 2006.
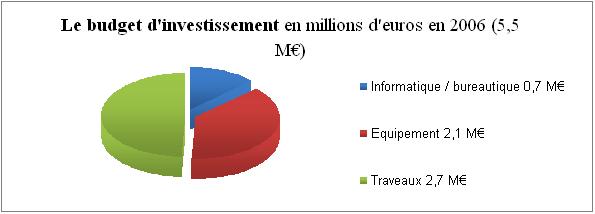
Figure
4 : Représentation graphique du
budget d’investissement en 2006.
I-4)-
Organisation de l’hôpital Ambroise Paré
Figure 5:
Plan de situation
de l’hôpital Ambroise Paré.
Voir Annexe 1 : Organigramme
d’organisation des services d’administration de l’hôpital.
II)-
Présentation de la Direction des Équipements
II-1)-
Organisation de la Direction des
Équipements
La Direction des Équipements de l’hôpital Ambroise
Paré est
constituée actuellement d’un Ingénieur Biomédical
chargé des équipements, d’un
responsable de bureau
d’achat, d’une secrétaire, d’un responsable d’atelier
biomédical et de quatre
techniciens biomédicaux qualifiés et compétents.
Le nombre du personnel dans la
Direction est suffisant, pour assurer leurs missions dans tous les
domaines de
sa responsabilité.
Voir Annexe
2 : Organigramme d’organisation de la Direction des
Équipements.
II-2)-
Missions de la Direction des Équipements
Les missions
de l’unité sont entre autres
de :
- Gérer
le budget d’investissement et d’exploitation
des équipements (biomédicaux et mobiliers) et suivre la
politique du maintien
du parc des équipements de l’hôpital,
- Elaborer et
mettre en œuvre le plan d’équipement
(définir les besoins, programmer et réaliser les achats et
l'intégration des dispositifs médicaux au sein de
l'hôpital),
- Organiser et
mettre en place une politique de
maintenance interne et externe des
équipements médicaux
(prévision
des dépenses de maintenance, achats des pièces
détachées, élaboration des
contrats de maintenance),
- Assurer la
sécurité des dispositifs médicaux,
organiser la matériovigilance au sein de l’établissement
et assurer la mise en
œuvre et le suivi des dispositions réglementaires relatives aux
dispositifs
médicaux actifs,
- Assurer
une veille technologique et réglementaire
dans le
domaine des technologies médicales et
assurer l’expertise et le conseil pour le corps médical,
- Participer
à des missions générales AP-HP et hors
AP-HP,
- Participer
à des
niveaux transversaux au sein de l’hôpital.
L'ingénieur
biomédical a pour
missions :
- Elaboration
et mise en œuvre d’un plan d’équipement (définir les
besoins, programmer et
réaliser les achats et
l'intégration des dispositifs médicaux
au sein de l'hôpital),
- Planification
des achats des équipements médicaux et mobiliers,
- Rédaction
des cahiers des charges pour les appels d'offre, marchés
négociés et mises en
concurrence,
- Conseil
technique à l'achat des équipements biomédicaux et
mobiliers auprès de la
A.G.E.P.S. et A.C.H.A.,
- Mise en
place de la démarche qualité au sein de la Direction des
Equipements,
- Accréditation,
- Conformité
aux normes et aux réglementations,
- Suivi de la
réglementation,
- Veille
technologique,
- Suivi des
prestataires extérieurs,
- Matériovigilance,
- Gestion de
management du personnel de la Direction,
- Suivi des
comptes de maintenance,
- Gestion des
contrats de maintenance.
Le
Responsable d’atelier biomédical intervient pour :
- Livraison et
installation de tous les équipements,
- Gestion de la
réforme de tous les équipements,
- Actions pour
favoriser l'utilisation optimale des dispositifs médicaux,
- Gestion du stock des
dispositifs médicaux, d’accessoires et de consommables,
- Gestion de la
maintenance des
équipements biomédicaux et de certains matériels
non médicaux,
- Gestion des
bons de commande et de réceptions relatifs à la
maintenance,
- Assurer la
traçabilité par Gestion de Maintenance Assistée
par Ordinateur (G.M.A.O.).
Les
techniciens ont pour rôle :
- Réception
de tous les équipements,
- Sécurité
et sûreté des dispositifs médicaux,
- Maintenance
préventive et contrôle qualité,
- Maintenance
corrective,
- Réforme
des équipements.
Chapitre
II
Présentation du Guide des Bonnes
Pratiques Biomédicales en Établissement de Santé
|
|
|
Chapitre II
Présentation du Guide des Bonnes
Pratiques Biomédicales en Établissement de Santé |
I)- Présentation
du Guide des Bonnes Pratiques
Biomédicales
Introduction
Le Guide
des Bonnes
Pratiques Biomédicales en Établissements de Santé [1] apporte les
éléments de réponse pour atteindre les objectifs
et remplir les missions d’un service biomédical hospitalier. Le
but de ce guide
est de fournir aux services biomédicaux,
les
références minimales auxquelles ils doivent satisfaire
pour considérer et
remplir correctement leurs fonctions, au mieux des
intérêts des personnels
soignant et indirectement des patients. Ce guide permet aux services
biomédicaux d'évaluer leurs pratiques quotidiennes par
rapport à l'outil d’auto
évaluation.
I-1)-
Contenu du Guide des Bonnes Pratiques
Biomédicales
Le Guide des
Bonnes Pratiques
Biomédicales en Etablissement de Santé (G.B.P.B.) est
composé de deux parties
principales :

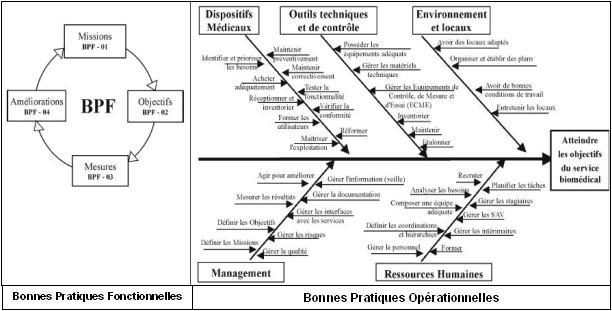
Figure 6 :
Processus des Bonnes Pratiques Biomédicales
fonctionnelles et opérationnelles.
I-1-1)-
Bonnes Pratiques Fonctionnelles (B.P.F.)
Actions
à
mettre en œuvre afin d’avoir en permanence une organisation apte
à
favoriser le développement et l’exécution
d’activités pertinentes et optimales
(réponses aux « pourquoi faire ? »).
BPF-01 :
Missions, BPF-02 : Objectifs, BPF-03 : Mesures, BPF-04 :
Améliorations.
I-1-2)-
Bonnes Pratiques Opérationnelles (B.P.O.)
Actions
à mettre en œuvre afin de réaliser des
activités pertinentes et optimales au sein du service
biomédical. Le but
est de répondre aux missions et objectifs définis dans
les bonnes pratiques
fonctionnelles (réponses aux « comment
faire ? »).
BPO-01 :
Processus de gestion des interfaces avec les
services,
BPO-02 :
Processus de gestion des risques et de la
qualité,
BPO-03 :
Processus de gestion du personnel,
BPO-04 :
Processus de gestion des locaux,
BPO-05 :
Processus de gestion et de suivi des MT &
ECME,
BPO-06 :
Processus de gestion et de suivi des DM.
I-2)-
Les avantages du Guide B.P.B.
[4]
- Très
proches du « métier » donc très
accessibles pour les acteurs qui les
mettent en œuvre,
- Visent
la réalisation d’activités suivant l’état de l’art
validé par les
« audits »,
- Le
guide exploite l’approche processus, l’auto évaluation et
l’amélioration
continue, alors :
-
Compatibilité forte avec les référentiels
d’accréditation H.A.S.
-
Compatibilité forte
avec les ISO 9001 et ISO 17025.
- Garantit
toutes les activités du
service,
- Facilité
de mise en œuvre,
- Contient
des exemples des indicateurs proposés.
I-3)-
Pourquoi mise en place du Guide
B.P.B.?
- Satisfaire
au mieux les exigences du client (personnel
médical et
para-médical),
- Apporter une confiance totale au client,
- Améliorer
l’image du service biomédical,
- Assurer
la sécurité du patient et personnel,
- Maîtriser les cadences de production en
améliorant
l’organisation
interne,
- Motiver
le personnel biomédical,
- Introduire
un cycle d’amélioration continu (Roue Deming).
II)- Présentation
de la grille d’évaluation
La grille d’évaluation [2] permet la mise en
évidence des actions d’amélioration à
mener, en mesurant les écarts entre les pratiques réelles
du service et les
références minimales du guide.
Elle permet
d’identifier et mesurer le progrès
réalisé depuis l’audit et ensuite, élaborer le
plan d’action nécessaire pour
augmenter le taux de conformité au guide.
La grille peut être
utilisée aussi bien pour une
auto-évaluation que lors d’un audit (évaluation et
contrôle de conformité).
Elle se compose d’un rappel des références minimales du
guide et pour chacune
d’entre elles, d’un nombre variable d’affirmations.
Rédigées sur le mode affirmatif,
elles sont plus directives et donc plus difficilement contournables.
Leur
formulation doit permettre d’éclaircir le lecteur sur le
résultat attendu de
chaque référence minimale tout en restant neutre quant
à la solution mise en
œuvre.
Cet outil permet de situer en un coup
d’œil sur
« une cartographie radar » ou un tableau
synthétique pour évaluer et
valider les « bonnes pratiques ». Il se
présente sous la forme
d'un classeur Excel composé de 7 onglets :
- Mode d’emploi :
Pour faciliter l’utilisation de la grille avec toutes les explications
et les
informations nécessaires.
- Grille
d’évaluation : se compose
d’un rappel des références minimales du
guide et d’un nombre variable d’affirmations pour chacune d’entre
elles.
- Grille de
cotation : Elle est
volontairement asymétrique et valorise les progrès
réalisés, chaque affirmation est affectée d’un
coefficient de pondération
permettant d’en distinguer l’importance relative au sein de la
référence
évaluée.
- Cartographie
radar : Elle permet une lecture
claire et synthétique des résultats obtenus
et met en évidence les actions prioritaires à engager.
- Fiche d’alerte :
Pour analyser les éventuels grands dysfonctionnements et
proposer des solutions
pour résoudre le problème.
II-1)-
Les avantages de la grille d’évaluation
- Fichier
Excel
rapide à utiliser,
- Grille
d’évaluation à cliquer,
- Calcul
automatique des résultats,
- Obtention
immédiate d’une synthèse en un coup d’œil sous forme d’un
tableau et d’une
cartographie radar,
- Contient
un exemplaire de fiche
d’alerte.
III)- Les
étapes d’utilisation du guide B.P.B.
Il existe plusieurs étapes
d’utilisation de ce référentiel afin d’avoir une
validation en « bonnes
pratiques » qui s’intègrent avec une introduction
d’une démarche globale
de qualité et d’amélioration. Les principales
étapes sont schématisées dans le
processus ci-dessous :
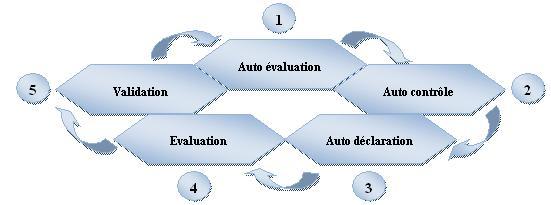
Figure 7 :
Processus des différentes phases d’utilisation du
guide B.P.B.
-
L’auto
évaluation
(grille
d’évaluation) est une méthode qui permet à une
équipe multi-professionnelle de
réaliser elle-même son propre diagnostic par rapport
à un référentiel déterminé
(GBPB). Elle permet la mise en évidence d’écarts par
rapport à des pratiques de
référence ou des objectifs d’organisation à
atteindre contenus dans ce
référentiel. Ainsi, elle est une aide à
l’élaboration de plans d’amélioration
de la qualité et s’intègre naturellement dans un cycle
d’amélioration continue
de la qualité.
- L’auto
cntrôle
(audit
interne) est
effectué grâce à la vérification
périodique
du système etaux actions correctives ou préventives que
l'on met en place
suite à des dérives réelles ou potentielles.
- L’auto
déclaration (déclaration
de conformité) correspond à une
attestation, émise par une première partie : le
service audité et l’audit
interne, indiquant qu’un produit, un processus ou un système de
management et
qualité est conforme aux exigences d’un
référentiel.
- L’évaluation
(audit
externe) est un examen
méthodique et indépendant qui permet d’évaluer si
ce qui est fait correspond
aux attentes et aux exigences exprimées dans un
référentiel. L’analyse des
observations effectuées au cours de cette évaluation
permet d’évaluer si les
dispositions mises en place sont efficaces et permettent d’atteindre
les
objectifs prévus. Elle peut aussi donner lieu à des
propositions ou des
recommandations en termes d’objectifs d’amélioration à
atteindre. Elle prend
aussi en compte les suggestions des audités. Il revient à
la structure évaluée
de définir les moyens les plus appropriés pour atteindre
les objectifs énoncés
dans le référentiel.
-
La
validation est une
confirmation par examen et apport de preuves tangibles que la mise en
œuvre ou
l’utilisation de tout processus, procédure, matériel ou
produit, activité ou
système permet réellement d’atteindre les
résultats escomptés.
IV)- Identification
de la problématique du sujet
Le QQOQCP
(outil
qualité) ci-dessous a permis de dégager et formuler la
problématique du
projet :

|
Chapitre III
Mise
en place des Bonnes Pratiques Biomédicales au sein de la
Direction
des Équipements |
Chapitre
III
Mise
en place des Bonnes Pratiques Biomédicales au sein de la
Direction des Équipements
|
|
Introduction
La Direction
des Équipements
doit connaître sa raison d’être, ses missions en
référence ou en complément des textes
réglementaires existants, ses relations
avec les parties prenantes.
La figure
ci-dessous explicite
ses missions. En effet, la Direction
intervient dans les différentes
phases du cycle de vie des équipements médicaux :
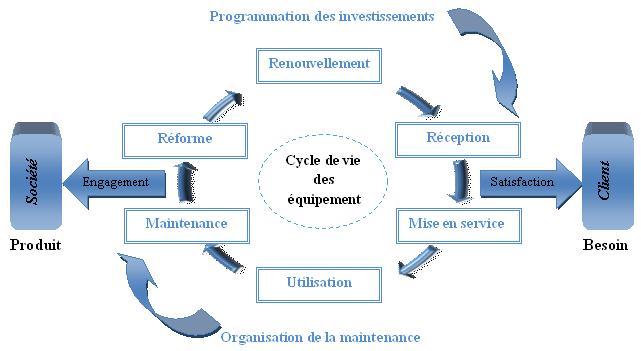
Figure
8 : la relation entre la Directiondes Équipements, le
fournisseur et
le client.
I)- Processus
de validation
Introduction :
L’objectif de
cette partie du projet est
d’étudier et de proposer un processus pour la validation de la
Direction des Équipements
(D.E.) en Bonnes Pratiques Biomédicales. Après
que la D.E. met en œuvre toutes les dispositions et les actions
nécessaires
pour satisfaire aux références et exigences du guide.
Avant de
faire une étude sur un processus
de validation, on pourrait se poser la question « pourquoi
valider ? »
L’origine du
guide vient en quelque sorte
du service qui souhaitait démontrer ses capacités
professionnelles et obtenir
une reconnaissance. Ce qui explique que le fait de
« se valider en Bonnes Pratiques
Biomédicales » permettrait une
reconnaissance d’autant plus forte dans l’hôpital. Et d’autre
part de valoriser
la profession et l’activité. De plus, le fait de pouvoir
« se
valider en B.P.B. » permettrait aux services
biomédicaux désireux de
s’initier dans une démarche qualité.
Suite
à plusieurs
réflexions, nous allons proposer un processus qui permet la
validation de la
Direction des Equipements en « Bonnes Pratiques
Biomédicales » :
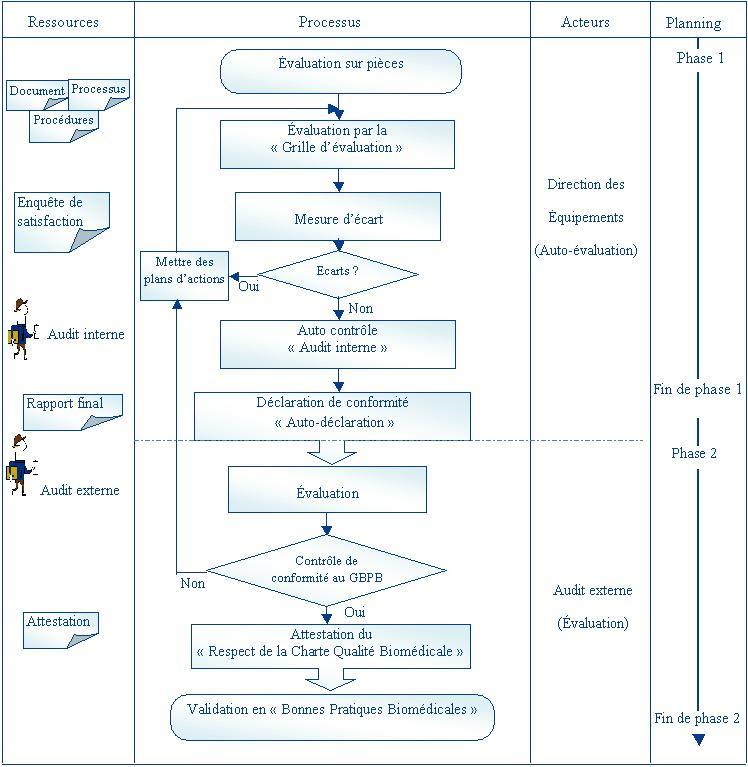
Figure 9:
Processus de mis en œuvre du Guide de
Bonnes Pratiques Biomédicales en Établissement de
Santé.
Cette
validation demande des différentes
préparations à mettre en œuvre, pour cela on a pris la
démarche suivante :
1.
Se concentrer
dès le début pour
identifier un seul objectif à atteindre,
2.
Réexaminer
les
références du
Guide des Bonnes Pratiques Biomédicales en Établissement
de Santé,
3.
Mise en place
d’une équipe de
travail (les personnes auditées),
4.
Définir le cadre d’action de l’évaluation et
ses finalités : procédures, processus…etc.,
5.
Analyser
les documents élaborés au
sein de la Direction des Équipements
qui seront examinés par la suite lors de l’évaluation,
6.
Élaborer le
questionnaire qui va permettre le recueil et la vérification
des données : une grille d’évaluation construite
à partir du Guide des
Bonnes Pratiques Biomédicales en Établissement
de Santé et une enquête de satisfaction pour
connaître à l’heure actuelle
le niveau de satisfaction des clients de l’année,
7.
Mettre en place des plans d’actions et des
actions
correctives afin de répondre le mieux possible aux exigences du
guide BPB.
retour sommaire
II) Les
différentes étapes de validation
en B.P.B.
II-1)- Auto évaluation
Introduction
- Définition : Examen systématique effectué par l’organisme
lui-même en vue de déterminer dans quelle mesure il est
capable de satisfaire à
un certain nombre d’exigences d’un référentiel.
L’auto
évaluation a pour objet d’évaluer
l’efficacité et l’efficience par rapport à des
critères définis dans le GBPB,
et d’établir des plans d’actions. Elle doit permettre au
responsable de la
Direction de vérifier la mise en œuvre des dispositions, leurs
adéquations aux
références du Guide B.P.B. pour maintenir et
améliorer la fonction et le
système qualité.
Réunion
d’ouverture (Au
début de l’auto évaluation)
La Direction
des
Equipements a organsinée avec PHILIPS deux journées de
formation pour
sensibiliser le personnel de la D.E. à la démarche
qualité. En suite, une
réunion d’ouverture a été organisée le 4
février 2008 sous la responsabilité du
chef de projet (Ingénieur biomédical) afin que tous le
personnel concerné soit
informé et impliqué dans la mise en œuvre de la
démarche qualité ; même la
Direction de l’hôpital a été informée. La
réunion comprend :
1.
Une courte
présentation
des méthodes à utiliser pour mener l’auto
évaluation,
2.
La
présentation mutuelle des participants (équipe
audités), y compris
un résumé de leur rôle et un encouragement à
une participation active,
4.
La
revue des objectifs de la validation en « Bonnes
Pratiques »
(amélioration, reconnaissance…),
5.
La
confirmation de la disponibilité de toutes les ressources, les
installations
nécessaires à l’équipe qui va mener
l’évaluation et
de l’identité de tous les documents.
En
règle générale, une
démarche simplifiée était présentée,
en fonction des objectifs et du champ de
l’évaluation et pour la
bonne réussite de notre
évaluation, il était indispensable que tout le personnel
de la Direction soit
motivé et impliqué, mais il fallait également que
l’équipe de la Direction de
l’hôpital soit engagée et même le service
Qualité.
Avant
d’entrer dans le détail de chaque
étape de l’auto évaluation, nous présentons le
processus ci-dessous :
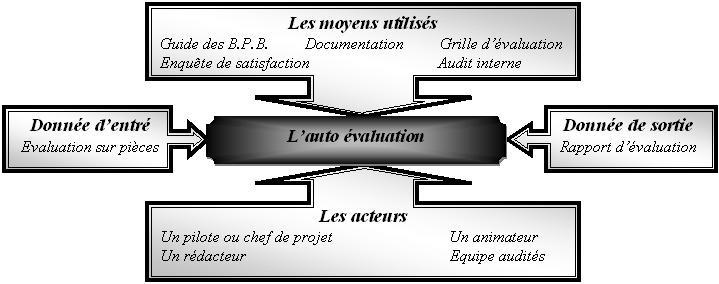
Figure 10 :
Processus de mise en œuvre
d’une auto évaluation.
II-1-1)-
Gestion d’archivage des documents
Etape 1 :
Rappel des différents documents du système qualité
Les différents
documents
qu’on utilise dans un système de gestion de la documentation
qualité
sont :
- Un manuel d'assurance
qualité est un
document qui énonce
la politique qualité et qui décrit l'ensemble du
système. La rédaction du
manuel d'assurance qualité débutera dès que le
nombre de procédures écrites
sera suffisant.
- Une
procédure
décrit la manière d'accomplir une activité. Une
procédure écrite comporte
généralement l'objet et le domaine d'application d'une
activité ; ce qui doit
être fait et qui doit se faire ; quand, où et comment cela
doit être fait ;
quels matériels, équipements et documents doivent
être utilisés ; comment cela
doit être maîtrisé et enregistré.
"C'est dire ce qu'on fait et faire ce que l'on
dit."
- Un processus est
un système
d’activités qui utilisent des
ressources pour transformer des éléments d’entrée
en léments de sortie.
- Une instruction de travail découle d'une procédure et
permet sa mise en exécution. La présentation des
instructions de travail est
identique aux procédures.
- Un
formulaire met en application
l'instruction de travail, il permet d'assurer que
toutes les actions sont réalisées et de les enregistrer
spécifiquement en vue
de la satisfaction des exigences de la qualité. Il permet de
suivre le
déroulement d'une méthodologie précise.
Etape
2 : Classement des
documents
La
maîtrise des documents et des données permet de formaliser
le savoir-faire des
acteurs de la Direction, de faciliter l'adaptation au poste de travail
et la
polyvalence dans le respect des compétences
réglementaires. La bonne gestion de
la documentation est le gage de l'assurance de la bonne maîtrise
de
l'information, en particulier concernant la transmission des
données aux autres
services et lors des changements d'équipe. Elle constitue donc
un des maillons
de la chaîne de maîtrise du risque au sein de
l'établissement de santé.
L’évaluation
sur pièces, nous a permis de vérifier et d’analyser tous les
documents élaborés au sein de la
Direction des Équipements qui
seront examinés par la suite lors de l’évaluation. Pour
faciliter le
développement de cette étape, nous avons regroupé
toutes ces données dans deux
listes en restant dans l’enveloppe de la bibliothèque
documentaire et
l’archivage de la Direction :
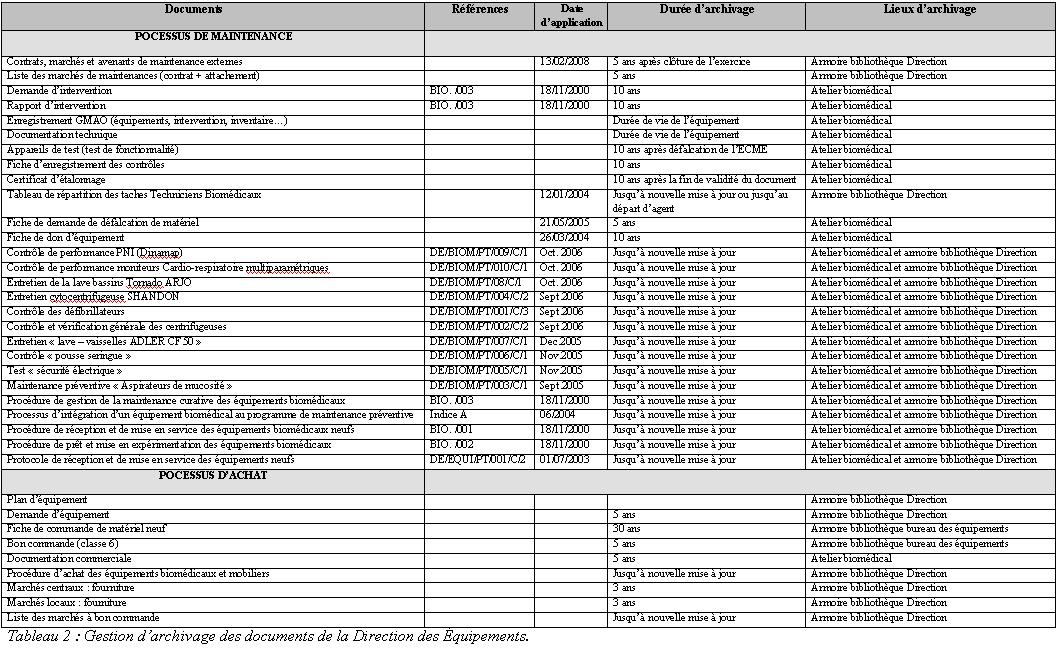
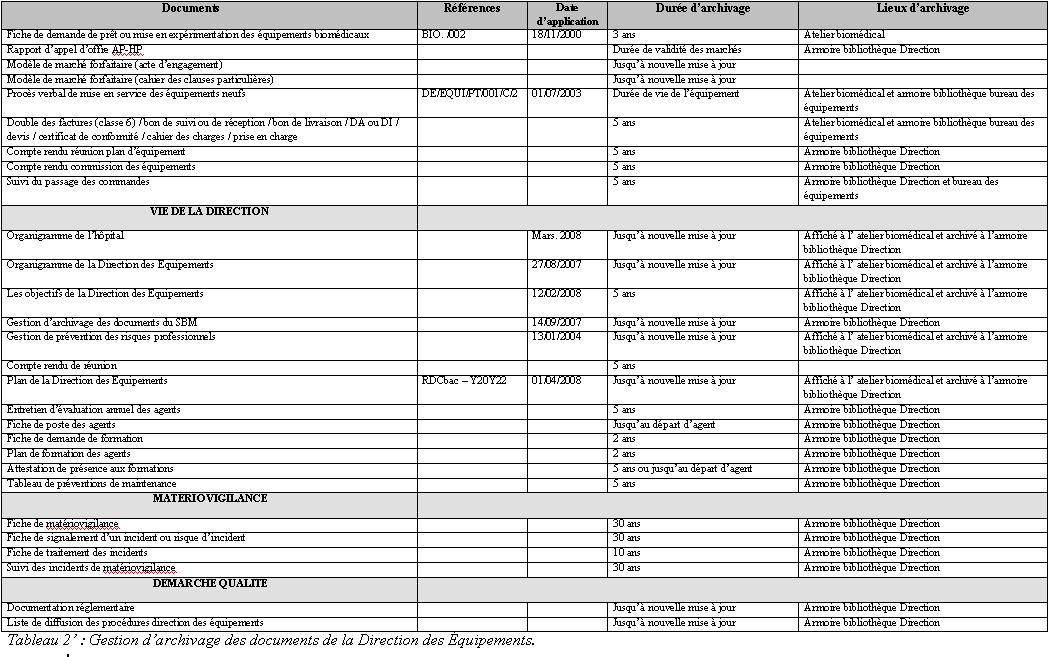
- Une liste de gestion d’archivage des documents de la
Direction avec la référence, la date d’application, le
lieu et la durée
d’archivage (Tableau 2 et 2’). Par rapport à cette liste,
nous avons rangé
tous ces documents dans un classeur au tri des affirmations des B.P. du
guide
avec la même codification alphanumérique. Ces documents
vont être utilisés
comme des preuves lors de l’évaluation
- Une
liste qui contient tous les autres documents qui
n’existent pas dans la Direction et le guide les exige, cette liste va
nous
aider dans l’étape : 3 et 4 pour mettre un calendrier de
rédaction des
documents.
Etape
3 : Rédaction des
procédures
La
maîtrise de la qualité est l'ensemble des techniques et
activités à caractère
opérationnel utilisés pour satisfaire aux exigences de la
qualité. Dans notre
cas, la maîtrise de la qualité passe par la
rédaction des procédures les plus
proches possibles de l'organisation mise en place par la D.E. des
pratiques professionnelles,
de l'enregistrement des différentes étapes
d’activités et de la systématisation
des pratiques.
De
même, la traçabilité et l'écrit sont les
deux caractéristiques indissociables
de la qualité, et pour répondre à ces
caractéristiques, j’ai rédigé ou
réactualisé certaines procédures et processus pour
être conforme aux exigences
du guide, avec la mise en place des indicateurs de performances pour
chaque
procédure qui permet de vérifier le taux de satisfaction
de la procédure, de
mesurer l’activité professionnelle et de voir les
non-conformités.
La
liste ci-dessous présente les différentes
procédures que j’ai réactualisées :
- Procédure
de
réception et de mise en service des équipements
biomédicaux neufs (cf. Annexe
7),

- Procédure
de
maintenance corrective des équipements biomédicaux (cf.
Annexe 9),

- Procédure de prêt
et mise en expérimentation des équipements
biomédicaux (cf. Annexe 11).

Une
deuxième liste qui présente les autres procédures
qui ont été réalisées et qui
n’existent pas dans la Direction des Équipements :
- Processus
d’achat
des petits et gros équipements biomédicaux et mobiliers
(cf. Annexe 6),

- Procédure
de
maintenance préventive et/ou de contrôle des
équipements biomédicaux (cf.
Annexe 8),

- Procédure
de
réforme des équipements biomédicaux (cf. Annexe
10),

- Procédure
d’accueil et d’encadrement des stagiaires (cf. Annexe 12).

Chaque
procédure comprend les paragraphes et la forme
suivante :
- Objet
: but de la procédure
- Domaine
d'application : où, quand, sur quoi l'objet de la
procédure s'applique
- Documents
et références : les éléments
auxquels il est fait appel pour le
processus décrit, ainsi que les normes et les textes
réglementaires régissant
la procédure
- Définitions
: les termes spécifiques utilisés dans la
procédure sont explicités afin de
faciliter la compréhension et communauté de langage
- Responsabilité :
l’autorité
et la responsabilité de chacun (qui fait quoi ?)
- Description : mode opératoire (qui
fait quoi ? et comment ?),
indicateurs de performances, logigramme.
- Annexe :
les
fiches et les documents satisfaisant la procédure.
Ces
procédures sont corrigées par le responsable de
l’atelier biomédical et validées par un groupe de
travail : Ingénieur
biomédical, chefs des services et/ou les cadres
supérieurs du service ou leurs
représentants et la cellule qualité chargée pour
l’approbation
des procédures.
Etape
4 :
Manuel Qualité
Le manuel
qualité (cf.
Annexe 13) a été
rédigé ; c’est le document le plus important d’un
système qualité. Cette
composante principale de la démarche qualité donne des
réponses par rapport aux
requis de la norme ISO 9001 en décrivant les
interprétations et les adaptations
dans l’organisation. C’est un véritable outil de communication
aussi bien à
l’intérieur qu’à l’extérieur de la Direction. Il
est en effet mis à disposition
des clients et il sert également d'outil de communication
interne. En outre, sa
rédaction permet à la Direction de définir :
- l'organisation,
les moyens et méthodes utilisées,
- le processus
du système de management de la qualité,
- la
politique qualité de la Direction des Equipements, le niveau de
service à fournir,
- l’objectif
qualité et la façon de procéder pour atteindre ces
objectifs,
- l’organisation
du système documentaire qualité,
- le rôle
du personnel dans la mise en oeuvre de la politique qualité,
- la
responsabilité, l'autorité de chaque membre de la D.E.,
- et apporter
la connaissance suffisante du système qualité,
- et donner la
confiance dans la conformité à la
référentielle qualité.
Sa structure
est adoptée selon la forme
du fonctionnement de la Direction, son organisation, son système
qualité et la
gestion de celle-ci. Il contient en grande majorité les
politiques et
engagements de la Direction. Sa lecture doit permettre au client
d'avoir une
connaissance suffisante du système qualité de son
fournisseur. Son objectif est
de décrire le système de management de la qualité
appliqué au sein de
l'organisme. Il est en cela "l'image écrite" de la Direction.
Rédiger
ce manuel qualité à la Direction
permet d'avoir un guide et les lignes directrices dans la suite de
l'implantation de la démarche qualité. Ce document a
été rangé dans un classeur
où sont classés tous les autres documents qualité.
II
-1-2)- La Grille d’évaluation
Introduction
La Grille
d’évaluation est un outil donnant une
réponse rapide et claire de la situation de la Direction des Équipements vis-à-vis des bonnes
pratiques biomédicales. Elle identifie les axes de
progrès où la D.E. devra
s’engager. Une fois l’état des lieux réalisé, la
Direction peut entreprendre la
démarche d’implantation du guide avec visibilité.
Etape 1 : Résultats de la 1ère
évaluation
Après
le remplissage de la grille d’évaluation qui mesure les
écarts
entre les pratiques réelles de la Direction et les
références minimales du
guide, les résultats étaient
présentés sous la forme d’une
cartographie radar en un coup
d’œil :
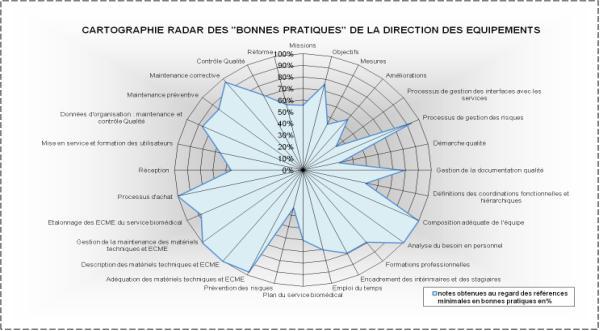
Figure 12 :
Cartographie radar des Bonnes Pratiques de la Direction des Equipements.
Etape 2 :
Analyse et recueil des données
Afin
d'exploiter au mieux l'outil d’auto
évaluation et de répondre le plus
précisément possible aux références
fixées
par ce dernier, le graphique ci-dessus (Figure 12) permet de visualiser
le
niveau de bonnes pratiques atteint sous la forme d’un graphe radar, ces
résultats sont des éléments pour :
- Identifier
les points faibles de la Direction
des Équipements,
- Aider
à prendre la décision pour définir la
stratégie de mise en place des Bonnes
Pratiques Biomédicales,
- Prioriser les
actions correctives à mettre en
œuvre (Tableau 4).
Les
résultats
globaux de la grille d’évaluation montrent que la Direction
s'inscrit déjà dans
une démarche qualité (note totale : 72,96 %). La
Direction a été en effet
engagée dans la phase d'auto évaluation à
formaliser, dans cette perspective,
un certain nombre de plan d’action. Cependant, le bilan de la grille
laisse
entrevoir certains points critique
et
faibles qui devront absolument être analysés dans le but
de maîtriser davantage
les processus de gestion des activités de la Direction ainsi que
la qualité des
prestations rendues aux différentes parties prenantes.
Ces points critique sont
identifiés et enregistrés de manière claire et
concise dans le tableau
ci-dessous :
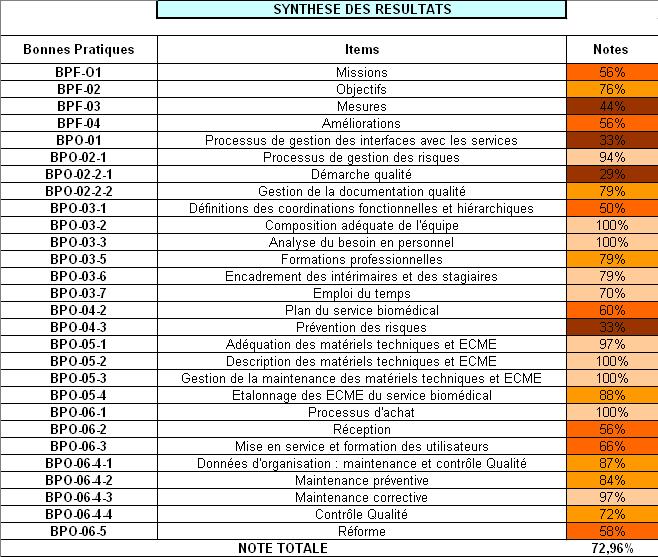
Tableau 3 : Synthèse
des résultats de la grille d’auto évaluation.
Ce tableau
récapitule la totalité des notes présentées
en pourcentage obtenues pour
l’ensemble des références minimales du guide, il facilite
la synthèse des
résultats et l’identification des points critiques qui s'obtient
en répondant à
ces quatre exigences :

Etape 3 : Mise en place d’un plan d’action
La mise en
évidence d’écarts entre l’observation et les
références du Guide des Bonnes
Pratiques Biomédicales en Établissement
de Santé nous a conduit à rechercher les causes des
dysfonctionnements qui
peuvent correspondre aux types suivants :
- Causes professionnelles,
- Causes
organisationnelles,
- Causes
managériales,
- Causes
institutionnelles.
Ainsi
que la réalisation de la grille a
permis de mettre en évidence les points forts et les points
faibles de la
Direction en regard du Guide des Bonnes Pratiques Biomédicales.
Afin
d'enclencher une véritable politique d'amélioration
continue de la qualité, il
apparaît judicieux de définir et mettre en place un plan
d'action corrective et
de revoir les non-conformités avec le chef du projet pour
obtenir des actions
de faits. Parmis les actions correctives réalisées :
- Affichage des
documents
Certains documents doivent être connus par
tout le personnel
de la Direction, c’est une caractéristique
indissociable du guide,
et pour être conforme à cette
exigence, on a
affiché :
- l’organigramme de
l’organisation des services
d’administration de l’hôpital (BPF-01) qui
définit le positionnement de la Direction des Équipements
dans l’hôpital (cf. Annexe 1),
- l’organigramme
hiérarchique et fonctionnel de la Direction des Équipements
(BPO-03-2) qui
définit la composition de la Direction et
la fonction de chaque membre (cf. Annexe 2),
- le
plan de la Direction des Équipements
(BPO-04-2) qui
définit les différentes zones de la
Direction qui sont dédiées à son activité (cf. Annexe 4),
- le
document de déclaration des
risques (BPO-02-1) pour limiter
et maîtriser les incidents associés à
l’exploitation des dispositifs médicaux
ou outils technologiques dont la Direction a la charge,
- les objectifs
de l’année en
cours (2008) (BPF-02) pour chaque membre de la Direction.
- Missions de la
D.E. (BPF-01)
Un
document
écrit et validé par la Direction de l’hôpital qui
définit les missions, les
moyens et les ressources de la Direction des Equipements était
mis sur Intranet
pour qu’il soit diffusé, accessible et connu par tous les
professionnels au
sein de l’hôpital.
- Gestion des
interfaces (BPO-01)
Le processus
de
gestion des interfaces avec les services semble maîtrisé
même si aucun document
formalisé ne retrace les interactions avec les parties prenantes
de la
Direction (service informatique, service technique, service
économique,…etc.),
sauf un seul document écrit qui existe, de gestion d’interface
entre la
Direction des Equipements et l’unité hygiène.
- Définitions des
coordinations
fonctionnelles et hiérarchiques (BPO-03-1)
Il n’existe
pas
une organisation des gardes et astreintes dans la Direction des Equipements,
mais par contre la DE a mis en place des équipements de secours
pour tous les
équipements critiques pour garantir la continuité de
l’activité des soins.
- Formations professionnelles
(BPO-03-5)
Définir
avec le
service de formation un processus qui permet d’évaluer la
formation du
personnel.
- Processus
de
gestion des locaux (BPO-04-2)
La gestion des
locaux vise à organiser, maintenir et entretenir
l’espace de travail mis à la disposition de l’atelier
biomédical, pour que ces
zones soient clairement identifiées, on a affiché des
étiquettes pour chaque
zone dédiée à l’activité de l’atelier :
- Zone de
stockage pour les
pièces détachées, le matériel de test, le
matériel de prêt, le matériel en
attente de réparation, le matériel réparé,
les accessoires,
- Zone
d’archivage des rapports
d’intervention, de la documentation technique, commerciale,
réglementation et
formation,
- Zone pour
réaliser les
interventions.
- Prévention
des risques
(BPO-04-3)
Le
comité
d’hygiène, de sécurité et des conditions de
travail se déplace dans les locaux
de la Direction des Equipements pour
contrôler les conditions du travail, ainsi que
le comité de lutte contre les infections nosocomiales pour
évaluer
l’application des mesures d’hygiène.
- Organisation de
la bibliothèque documentaire (BPO-06-4-1)
La bibliothèque documentaire de l’atelier
biomédical doit
être organisée, disponible et facile à utiliser par
tout le personnel
biomédical, pour cela, on a :
- Organisé
la documentation
commerciale dans une nouvelle armoire, triée par ordre
alphabétique par
rapport au nom des sociétés,
- Mise à
jour de la
documentation réglementaire et classement de ces documents dans
des classeurs
par rapport à la date et le domaine d’application.
Le
développement
d'une démarche qualité est un projet à long terme.
Il suppose l'appropriation
progressive des principes et des méthodes par l'ensemble des
professionnels de
l'établissement et un apprentissage de nouveaux savoir-faire.
La
démarche doit
d'abord s'envisager de façon progressive. Ce principe de
progressivité conduit à
se concentrer sur des priorités, c'est-à-dire sur les
points qui produiront les
améliorations les plus notables. [5]
Le tableau
ci-dessous (Tableau 4)
présente ces points ainsi les solutions que nous avons
proposées pour résoudre
les dysfonctionnements et les améliorer pour être
conforme aux exigences
du guide :
|
Plan d’action
|
|
Référence
|
Sujet
|
Proposition
|
Résultat
|
|
BPF-01
|
Missions
|
Mr. Belhanini : rédiger un document
écrit et validé par la direction qui définit les
missions, les moyens et les ressources de la D.E. et le mettre sur
Intranet.
|
Fait
|
|
BPF-03
|
Mesures
|
Mlle Chtiha : réaliser une Enquête de
satisfaction.
|
Fait
|
|
Mlle Chtiha : rédiger un processus d’auto
évaluation.
|
Fait
|
|
BPO-02-2-1
|
Démarche
qualité
|
Mlle Chtiha : Rédiger un document qui
définit la politique qualité de la Direction.
|
Fait
(manuel qualité)
|
|
Rédiger un document définissant
les missions et les responsabilités du personnel en
matière qualité.
|
|
|
Mlle Chtiha : Réaliser et enregistrer l’auto
évaluation.
|
Fait
|
|
Réaliser et enregistrer les audits
internes.
|
En cours
|
|
BPO-02-2-2
|
Gestion de la
documentation
|
Mlle Chtiha : Un système documentaire
qualité : Manuel qualité.
|
Fait
|
|
BPO-03-5
|
Formation professionnelle
|
Réaliser des supports
récapitulatifs des qualifications, habilitations, formations et
expériences de chaque membre du personnel.
|
|
|
BPO-03-1
|
Définition des
coordinations fonctionnelles et hiérarchiques
|
Faire une organisation des gardes et
astreintes.
|
|
|
BPO-03-6
|
Encadrement des
intérimaires et des stagiaires
|
Mlle Chtiha : rédiger une procédure
d’accueil et d’encadrement des stagiaires.
|
Fait
|
|
BPO-04-2
|
Plan du service
biomédical
|
Mlle Chtiha : Établissement et affichage
d’un plan de la Direction des Équipements.
|
Fait
|
|
|
|
Mlle Chtiha : Identifier les différentes
zones d’activités de l’atelier avec des étiquettes.
|
Fait
|
|
BPO-06-1
|
Processus d’achat
|
Mm Martin: Rédiger une procédure d’achat.
|
En cours
|
|
|
|
Mlle Chtiha : réaliser un processus d’achat
des petits et gros équipements biomédicaux et mobiliers.
|
Fait
|
|
BPO-06-2
|
Réception
|
PV de contrôle de conformité par
rapport à la commande est réalisé lors de la
réception des D.M.
|
|
|
Mlle Chtiha : mise à jour de procédure de
réception et de mise en service des équipements
biomédicaux neufs.
|
Fait
|
|
BPO-06-4-1
|
Données
d’organisation pour la maintenance et le contrôle qualité
|
Processus de gestion des stocks permettant
d’optimiser les moyens par rapport aux besoins.
|
|
|
BPO-06-4-2
|
Maintenance
préventive
|
Mr. Zanzouri : 3 Protocoles de maintenance
préventive.
|
Objectif 2008
|
|
Mr. Llech : Tableau de bord pour le suivi de la
maintenance.
|
Fait
|
|
Mr Llech : Planning des maintenances
préventives.
|
Fait
|
|
Mlle Chtiha : rédiger une procédure
de maintenance préventive.
|
Fait
|
|
BPO-06-4-3
|
Maintenance corrective
|
Mr. Llech : Protocole de maintenance préventive
du respirateur Sero I.
|
Objectif 2008
|
|
Mr. Llech : Protocole de maintenance
préventive et corrective.
|
Objectif 2008
|
|
Mlle Chtiha : rédiger une procédure
de maintenance corrective.
|
Fait
|
|
Mr. Tourat :
Protocole de maintenance.
|
Objectif 2008
|
|
BPO-06-5
|
Réforme
|
Mr. Tourat et Mlle Chtiha : Procédure de mise en
réforme des équipements biomédicaux.
|
Fait
|
|
|
|
Réaliser un processus de non
conformité
|
|
|
|
Tableau 4 : Les différents points
faibles de la Direction des Equipements
Etape
4 : Comparaison avec une
moyenne
Une fois que
l’état
des lieux était réalisé (Figure 12), une
comparaison a été faite entre nos
résultats d’auto évaluation et une moyenne comparative "Bonnes Pratiques
Biomédicales"
de
certains services biomédicaux (41 hôpitaux dont 9
Québécois) de l’année
2007 [6],
cette comparaison nous a permis de se situer par rapport
à la moyenne
des réponses reçues (benchmarking) et d’aspirer les voies
de progrès possibles.
La
cartographie ci-dessous présente les résultats de cette
comparaison :
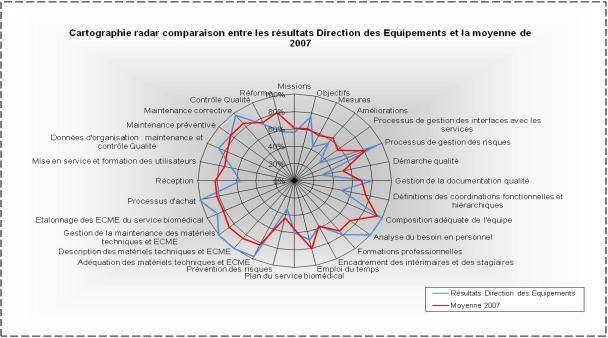
Figure 13 : Cartographie radar des Bonnes Pratiques
Biomédicales de la
Direction des Équipements et la moyenne de 2007.
Après,
l’analyse de la cartographie ci-dessus, il est remarquable que la
Direction
soit bien située par rapport à la moyenne comparative "Bonnes Pratiques
Biomédicales"
des
différents services biomédicaux de l’année 2007.
En revanche, elle laisse
entrevoir certains points faibles qui devront absolument être
traités en
priorité (Etape 3 et 4). Cette auto évaluation fait
l'objet de comptes rendus
enregistrés.
Etape
5 : Indicateurs de
performances
Définition :
Un indicateur est un " événement
" observé, prélevé, mesuré,
déterminé par le calcul permettant
d'identifier qualitativement ou quantitativement une
amélioration positive ou
négative du comportement d'un procédé.
L’intérêt
des indicateurs est de se
situer par rapport à des objectifs, mesurer les
activités, de s’évaluer par
rapport à la distance qui sépare la Direction des
Equipements à ses objectifs
et surveiller les processus.
Pour
répondre à l’objectif fixé, nous avons bâti
un tableau de bord (Tableau 5) qui
assure le suivi de ces indicateurs et permet une amélioration
continue (un
cycle PDCA (Plan-Do-Check-Act).
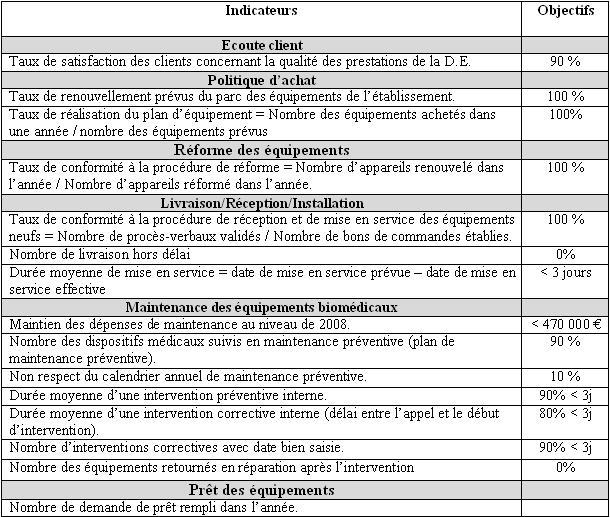
Tableau 5 :
Les indicateurs de performances de la
Direction des Equipements
Ces indicateurs sont
définis par :
- Déclinaison
des objectives qualités du
service,
- Processus,
- Valeur
cible à atteindre,
- Stables
dans une période de temps défini
pour permettre la mesure de la progression.
Deux
méthodes de recueil de ces
indicateurs ont été mises en place :
- L’enquête de
satisfaction : l'opinion de tous ceux et celles qui sont en
contact
direct avec la Direction est une source précieuse de
renseignements.
- La GMAO : est
un outil informatique capable de prendre en compte un
événement par le biais de
ses composantes techniques et financières. Il permet de
faciliter l'accès aux
données, leur saisie et leur stockage.
Les informations
provenant
des indicateurs de qualité doivent être exploitées.
En effet, on ne mesure pas
pour le plaisir de mesurer, mais à partir des mises en
évidences des
dysfonctionnements faites grâce aux indicateurs de
qualité, l'attitude va
consister à agir sur les causes et les éliminer.
Le tableau
ci-dessous présente une liste de
proposition des indicateurs de suivi qui permet à la Direction
d’atteindre ses
objectifs :
Tableau
6 : Les indicateurs de suivi de la
Direction des Equipements
Etape 6 :
Réunion de clôture (À la fin de
l’auto évaluation)
Suite
à l’auto évaluation, on a organisé trois
réunions de clôture. Ces
réunions sont dirigées par le Chef de projet
(Ingénieur biomédical), en
présence des personnes présentent au cours de la
réunion d’ouverture, les
réunions ont pour objectif de :
1.
Revoir les
constats et toutes les autres
informations appropriées recueillies pendant l’auto
évaluation,
2.
Présenter
les constats et conclusions de
l’auto évaluation,
3.
Présenter
les résultats de l’enquête de
satisfaction,
4.
Prendre des
décisions validées par
l’ensemble de l’équipe.
5.
Vérifier
l’état d’avancement de
différentes actions mise en œuvre.
II-1-3)-
Enquête de
satisfaction
Introduction
L’écoute
client
est un principe important de la démarche qualité, la
satisfaction du client est
directement liée à cette écoute. L’écoute
client doit faire l’objet d’un
processus de récolte d’informations qui mesure non pas les
réclamations client
mais sa satisfaction. Qu’elle soit positive ou négative, la
mesure de la
satisfaction permet de corriger les points de mécontentement et
de pérenniser
les points positifs.
« Le client est au centre de la démarche
qualité ».
II-1-3-1)-
Objectif de l’enquête
Une
enquête de satisfaction (cf.
Annexe 3) a été élaborée pour la
première fois à la D.E. et envoyée aux
différents chefs de pôle et cadres de service de
l’hôpital afin de connaître, à
l’heure actuelle, leur niveau de satisfaction aux différentes
activités de la
Direction et de comprendre leur besoins afin de mieux répondre
à leur attentes.
Cet outil
nous a permis de recenser les
problèmes vus par nos clients et mettre en place un plan
d’amélioration de la
qualité pour les satisfaire et aussi mettre des indicateurs de
performances et
des objectifs pour répondre à leurs besoins.
II-1-3-2)-
Démarche mise en œuvre
La
démarche de qualité n'a de sens que si
elle est conduite dans une dynamique globale d'établissement et
accompagnée de
la Direction de l’hôpital et les autres services. En effet,
l'analyse détaillée
des références minimales du Guide des Bonnes Pratiques
Biomédicales fait
apparaître, à juste titre, la Direction dans un tissu
relationnel relativement
étendu qui conditionne fortement la bonne application de ses
actions.
Etape
1 :
Déroulement de l’enquête
Cette
enquête,
concernant la qualité des prestations de la Direction au cours
des 12
derniers mois écoulés de l’année 2007/2008,
composée de 18 questions. Elle a
été envoyée par mail le 20 mars 2008 à tous
les chefs de
pôle et les cadres de service de l’hôpital avec une date
limite de retour
de réponse jusqu’au 22 avril 2008.
Sur 89 chefs de pôle et cadres de service (40 services
et 4 pôles), seuls
28 ont répondu et 2 autres services ne sont pas concernés
par ce questionnaire.
Le taux faible (31%) de réponse exploitable sur les
questionnaires envoyés est
expliqué par le fait que certaines réponses
étaient collégiales (2 à 3
personnes par réponse).
Les
étapes ci-dessous se sont révélées
nécessaires pour analyser et mettre en place un plan d'actions
à la fois complet
et cohérent afin d’assurer la satisfaction des clients :
- Relecture
attentive des réponses de l’enquête,
- Analyse des
résultats « question par
question » avec calcule des notes,
- Repérage
et identification des points critiques,
- Construction
d'un plan d'action assurant une
conduite d’amélioration efficace : détermination des
actions prioritaires
à engager selon un planning à plus ou moins long terme
pour répondre aux
besoins des services médicaux, médico-techniques,
logistiques,
- Validation du
plan d'actions par l'Ingénieur
biomédical,
- Vérification
de l’état d’avancement des
résultats obtenus.
Etape
2: Analyse de
l’enquête
L’enquête
de satisfaction a été réalisée
suivant 5 niveaux :
- Satisfait :
le service est satisfait à plus
90%, l’activité est bien maîtrisé,
- Plutôt
satisfait : le service est
moyennement satisfait entre 75% et 90%, l’activité est
suffisamment maîtrisée,
mais toujours il y a des améliorations,
- Plutôt
pas satisfait : le service est
moyennement satisfait entre 50% et 75%, l’activité est
moyennement maîtrisée,
il faut corriger cette défaillance dès que possible,
- Pas du tout
satisfait : le service n’est
pas satisfait à moins de 50%, l’activité est
insuffisamment maîtrisée, il faut
revoir ce point en priorité et proposer des actions correctives,
- Non
concerné : le service n’est pas
concerné par cette question.
A chaque
critère précédent correspond une cotation :
- Satisfait :
« 3 »
- Plutôt
satisfait : « 2 »
- Plutôt
pas satisfait : « 1 »
- Pas du tout
satisfait : « 0 »
Une
difficulté de calcul des notes s’est
avérée délicate étant donné que le
taux de réponse pour chaque question est
différent. Pour que les notes puissent être
comparées entre elles et
interprétées correctement les données de cet
enquête, il est nécessaire de
comprendre comment les données ont étés
uniformisées afin de les représenter
ensemble.
Si l’on
considère chaque note figurant
dans le tableau ci-dessous (Tableau 7) celle-ci correspond à la
valeur N :

N1 est un
ratio (ex : 63/23 pour la question
1), qui nous informe que sur
les 28 questionnaires retournés remplis. Seulement 23
réponses ont été
renseignées sur les 4 niveaux pour cette question
(concernée) et 5 sont non
concernées, la note trouvée est égale à N1
= 2,78.
Si nous
traitons une autre question, il
est possible de rencontrer le ratio N1 = 69/26.
La note
totale de la Direction des
Equipements, s'obtient on
appliquant la règle suivante :

Le tableau
ci-dessous permet une lecture claire, synthétique des
résultats et des notes
calculées et met en évidence des actions prioritaires
à
engager « question par question » :
Tableau
7 : Résultats de l’enquête de satisfaction
Note :
Pour retrouver les questions vous pouvez consulter le questionnaire (cf. Annexe 3).
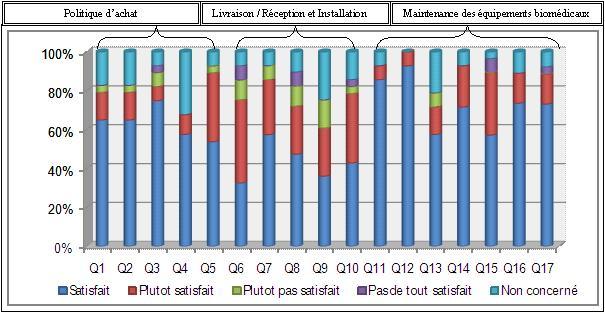
Figure 14 :
Taux de satisfaction des services pour chaque question de
l’enquête.
Note :
Pour retrouver les questions
vous pouvez consulter le questionnaire (cf. Annexe 3).
À la
fin de l’enquête, une question est posée d’une
façon générale (Q18), pour savoir le taux de
satisfaction des clients
concernant la qualité globale des prestations de la Direction
des Equipements,
les résultats sont tracés sous la forme suivante :
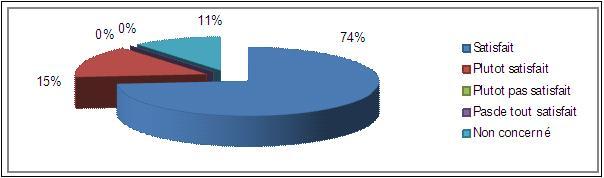
Figure 15
: Taux de
satisfaction concernant la
qualité
des prestations de la Direction
Les
résultats de l’enquête ont été
présentés dans une réunion de service à
l’ensemble de la Direction de manière à
faire un bilan et se fixer des objectifs simples et rapidement mis en
place et
même dans une réunion de Direction à l’ensemble des
cadres des services.
Au regard du
graphe récapitulatif (Figure
14) et les résultats que nous avons eu, il apparaît que
l'organisation de la
Direction présente quelques dysfonctionnements au niveau de la
livraison, la
réception et l’installation des équipements neufs
(chapitre B).
Ce
dysfonctionnement est dû au manque
d’informations lié au suivi de la livraison et des
problèmes de communication
entre le livreur et les services, en conséquence, le chef ou le
cadre de
service n’est pas présent pour réceptionner le
matériel ou le service n’est pas
disponible pour effectuer l’installation.
Etape
3 : Mise
en
place des actions correctives
L'ensemble
des améliorations correctives
à apporter à la Direction et correspondant aux points
critiques identifiés
précédemment (Figure 14) et les commentaires inscrits
dans les réponses des
chefs de pôle et cadres de service, ces points sont
retracés ci après avec
les conduites à tenir qui nous semblent les plus
judicieuses et les plus faciles à mettre en œuvre pour
répondre aux exigences
et besoins de nos clients :
- Tableau
de répartition des délais d’intervention :
Un tableau de
répartition des délais
d’intervention a été réalisé (cf. Annexe 14), le classement a
été fixé avec les
services en fonction des niveaux d’intervention, d’urgences et du type
d’équipement, avec un système de couleurs. Ce tableau va
être mis en place et
diffusé aux services afin de leur permettre de savoir la date de
passage du technicien
biomédical pour intervenir.
- Demandes
d’intervention :
Dans le cadre
de
la gestion des demandes d’intervention et de réparation,
l’Ingénieur biomédical
souhaite que OPTIM (GMAO) soit disponible sur Intranet afin
d’être utilisé par
les services. En effet, ils pourront émettre leur demande
d’intervention en
complétant le tableau et par rapport à l’urgence et
priorité le technicien peut
répondre à cette demande et informe le service par la
date et l’heure de
passage approximative pour réaliser l’intervention. Cette date
est donnée dans
le tableau de répartition des délais d’intervention.
- Tableau de
répartition des tâches :
Réalisé
un tableau de répartition des
tâches précisant la personne responsable de la nature de
l’intervention (qui
fait quoi ?). Ce tableau va être mis en place et
diffusé aux services afin
de leur permettre de mieux cibler leurs demandes.
- Livraison
/
Réception et Installation :
Cette
problématique s’aperçoit au niveau
de la livraison. Il n’existe pas une planification réelle de la
livraison entre
la DE et le service. Deux solutions étaient proposées
pour résoudre ce
dysfonctionnement :
- Une
fois que le fournisseur contacte l’atelier biomédical pour
prendre le R.D.V. de
la livraison. L’A.B. doit transmettre cette information (date et heure
de la
livraison) à l’avance au service concerné par
téléphone et/ou par e-mail avec
accusée de réception.
- Dans
le cas où le fournisseur n’a pas pris le R.D.V., l’atelier
biomédical doit
appeler le fournisseur deux semaines avant la date limite contractuelle
de la
livraison pour prendre le R.D.V. en concertation avec les cadres de
service.
Les actions
correctives préconisées
démontrent l'importance de la coordination des différents
acteurs et parties
pertinentes pour assurer la sécurité et la qualité
des soins délivrés au
patient.
La
réalisation du processus ci-dessous
inscrira durablement la Direction dans une démarche
d'amélioration continue de
la qualité et lui garantira des pratiques professionnelles
reconnues par
l'ensemble des acteurs médicaux et para-médicaux :
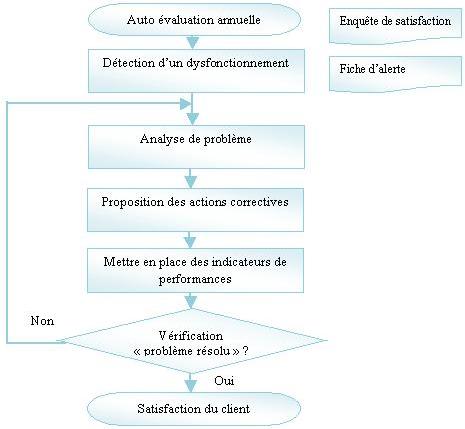 Figure 16
: Processus d’action
à mettre en œuvre
pour résoudre un dysfonctionnement.
Figure 16
: Processus d’action
à mettre en œuvre
pour résoudre un dysfonctionnement.
Etape
4 :
Processus d’auto évaluation
 Un processus
d’auto évaluation ci-dessous est mis en
place pour assurer le cycle d’amélioration continue et
vérifie tout les autres
processus qui s’intègre avec la mission et les pratiques
professionnelles de la
Direction :
Un processus
d’auto évaluation ci-dessous est mis en
place pour assurer le cycle d’amélioration continue et
vérifie tout les autres
processus qui s’intègre avec la mission et les pratiques
professionnelles de la
Direction :
Figure 17 : Processus d’auto évaluation.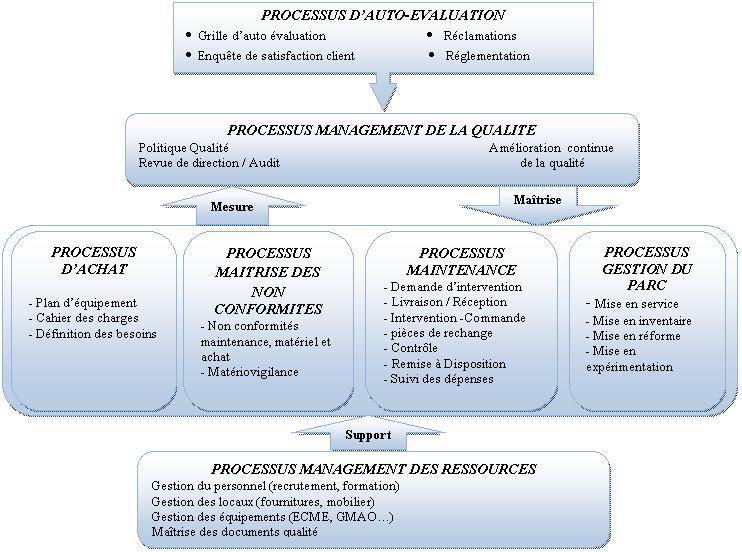
Réussir
une démarche qualité au sein de la Direction
des Équipements nécessite des
actions selon
le concept de la roue de DEMING (voir page 93) appliquée au
service d’une façon
d’agir en vue d’un cycle d’amélioration continue et d’utiliser
les moyens
suivants :
- Moyens pour
vérifier : utilisation
de l’auto évaluation et les examens
d’évaluation (audit) pour déterminer si les dispositions
préétablies sont mises
en œuvre de façon efficace.
- Moyens pour
améliorer :
élaboration
d’une enquête de satisfaction qui permet de recenser les
problèmes vus par
nos clients et de mettre en place un plan d’amélioration de la
qualité pour les
satisfaire avec des indicateurs de performances et des objectifs pour
la
mesure.
- Moyens pour
prouver :
les
enregistrements, formulaires, compte rendu, procédures et les
rapports de
l’auto évaluation…etc. sont nécessaires comme
épreuve lors d’un examen
d’évaluation et pour assurer la traçabilité et la
bonne transmission de
l’information.
II-2)-
L’auto
contrôle
Introduction
L'assurance
de la qualité est l'ensemble
des activités préétablies et
systématiques mises en œuvre dans le cadre du système
qualité pour donner
confiance dans sa capacité à satisfaire un
système, et permettre à ce système
de s'auto contrôlé.
"L'assurance de
la qualité c'est la démonstration de la qualité"
II-2-1)-
Réalisation d’auto contrôle
L'auto
évaluation a été réalisée sur
l'initiative du responsable de la Direction des Équipements
avec la participation du
personnel biomédical. Le responsable de la cellule
qualité de l'établissement
doit être associé à cette démarche comme un
audit interne. Elle a pour but
d'inciter le personnel à se situer par rapport à
l'état d'avancement de la
démarche et de réaliser un premier contrôle et
vérification.
II-2-2)-
Résultat de la 2ème auto évaluation
Une deuxième
auto évaluation a été réalisée,
afin de vérifier l’état d’avancement des modifications
apportées et les actions
correctives qui mènent d’avoir pour chaque affirmation de BP de
la grille
d’évaluation une note supérieure ou égale à
0,5 (50%) et d’évaluer les
pratiques et le niveau de satisfaction de la Direction par rapport au
guide
BPB. Le graphe ci-dessous présente les résultats que nous
avons obtenus :
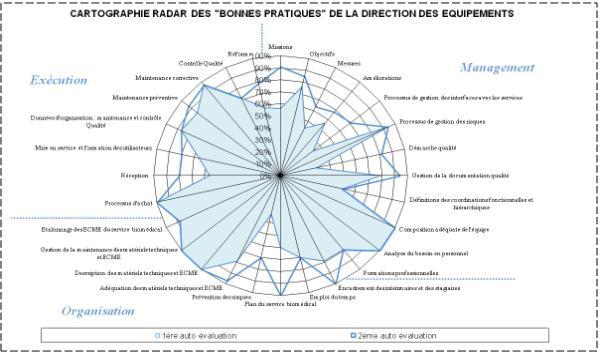
Figure 19:
Cartographie radar des Bonnes
Pratiques de la Direction des Équipements.
-
Conclusion :
Les
résultats de l’auto évaluation indique globalement
après les actions
correctives mises en place que toutes les prestations sont suffisamment
maîtrisées (notes supérieures à 50%) et la
note total de l’ensemble des B.P.
est 85,38%.
II-3)- Auto déclaration
Introduction
La
Déclaration de Conformité correspond à
un projet de norme ISO 17050, élaborée par la
Comité pour l’évaluation de la
conformité (CASCO) de l’Organisation Internationale de
Normalisation
accompagnée des documents d’appui relatifs à la norme ISO
17049 pour augmenter
la confiance accordée à la déclaration [7].
II-3-1)-
Déclaration de
Conformité
L’objectif
de cette déclaration est de donner l’assurance que l’objet de la
déclaration
est conforme aux exigences spécifiées auxquelles elle
fait référence. Elle
indique clairement qui est responsable de cette conformité et de
cette
déclaration. Une fiche de déclaration de
conformité (Annexe 5) a été
fondée sur une auto évaluation et un auto contrôle.
II-4)-
Validation en B.P.B.
La validation
"Bonnes
Pratiques" du service audité s'obtient en répondant aux
deux exigences de la grille de cotation ou le tableau de
synthèse :
-
Notes
supérieures à 0,5 (50%) pour chaque B.P.
-
Note
total pour l’ensemble des B.P. équivalent à minimum de
90%.
Le
titre validation "Bonnes Pratiques" doit être
présenté sous la forme
d'un certificat signé et daté conjointement par l’audit
et par le chef de la
Direction des Équipements
attestant la conformité aux exigences du guide des B.P.B. ainsi
la validation de
la Direction en « Bonnes Pratiques
biomédicales ».
D’autre
part comme précisé dans la partie II, les
différentes étapes de validation en B.P.B., nous
reprenons dans le
tableau ci-dessous, les principaux processus qui mènent à
la finalité et
l’objectif voulu « validation en BP » :
Figure
21 : Schéma de validation en « Bonnes Pratiques
Biomédicales »
Dans
notre cas, la Direction n’est pas encore prête pour faire
l’évaluation d’audit,
en attendant que les autres actions d’amélioration soit misent
en place pour
répondre aux exigences de la grille de cotation
mentionnées précédemment.
La validation
en « Bonnes
Pratiques » n’est pas un examen ou un concours que passe
chaque service
mais plutôt un travail de fond mobilisant l’ensemble de ses
personnels autour
d’un objectif commun : mieux travailler ensemble pour assurer une prise
en
charge de la qualité.
la mise en
œuvre des actions correctives
suite à l’auto évaluation a permis une
amélioration sensible du Système de
Gestion de la Qualité de la Direction des Equipements et
à l’aide du Guide des
Bonnes Pratiques Biomédicales en Etablissements de Santé,
la Direction peut
soutenir ses membres dans leur travail quotidien, en leur donnant des
recommandations techniques minimales afin de garantir des performances
satisfaisantes dans l’exploitation des équipements
biomédicaux et introduction
d’un cycle d’amélioration continu.
Ainsi,
l’utilisation de la grille
d’évaluation a permis de vérifier la mise en œuvre des
dispositions, leurs
adéquations aux références du guide des B.P.B.
pour maintenir et améliorer le
Système de Gestion de la Qualité au service du patient.
L’objectif
de la mise en place de ce guide est de
faire progresser la Direction vers une reconnaissance professionnelle
interne
au sein de l’hôpital et externe entre les hôpitaux de
l’AP-HP.
Références
Bibliografiques
|
Bibliographie
citée au
rapport
[1]
Guide des Bonnes Pratiques Biomédicales en
Etablissements de Santé, G.FARGES (UTC), G.WAHART (Pdte AFIB),
JM.DENAX (Pdte
AAMB), H.METAYER (Pdte ATB), et 45 co-auteurs, ITBM-RBM News, Ed
Elsevier, novembre
2002, vol 23, suppl. 2, 23s-52s, ISSN 1297-9570. URL : https://www.utc.fr/~farges/bonnes_pratiques/bpb.htm#guide
[2] Contribution
à la
démarche de validation "bonnes pratiques biomédicales" en
établissement de santé : la grille
d'évaluation, A. Guyard, L. Tamames, G.
Farges (UTC), ITBM-RBM News, Ed Elsevier, 2004, vol 25, n°2 (date
de
consultation: 20/02/08). URL : https://www.utc.fr/~farges/dess_tbh/03-04/projets/guyard-tamames/grille_eval_GBPB.htm
[3]
Présentation de l'hôpital Ambroise Paré. URL : http://www-aprnet/interne.php?type=preshop
(date de consultation: 11/02/08)
[4]
Référentiel métier et qualité en
ingénierie
biomédicale hospitalier, partie I (pp : 20) et partie II
(pp : 34),
Gilbert
Farges, Extranet
Master MTS,
URL : https://www.utc.fr/~farges/
[5] « Principes
de mises en œuvre d'une démarche qualité en
établissement de santé ».
Référence ANAES – Avril 2002 p.73 –
[6]
Moyennes
comparatives "Bonnes Pratiques Biomédicales", partie : moyennes
2007 (41 hôpitaux dont 9 Québécois) :
moyennes_BPB_2007.pdf
(date de
consultation: 25/02/08)
URL :
https://www.utc.fr/~farges/bonnes_pratiques/bpb.htm#bench
[7]
Projet de norme ISO 17050, Exigences générales pour la
déclaration de
Conformité du fournisseur, ISO/CEI CD 17050 du 16 avril
2002.Projet de norme
ISO 17049, Exigences générales relatives à la
documentation venant à l’appui de
la déclaration de conformité du fournisseur, ISO/CEI CD
17049 du 15 avril 2002. Edition
ISO/CASCO, Comité pour l’évaluation de la
conformité. URL : http://www.iso.ch/iso/fr/comms-markets/
Relative
aux rapports des étudiants Biomédicaux
- Processus
de validation d’un service biomédical en bonnes pratiques
biomédicales: Emmanuel
BERENGER et David BATTIN, Projet
DESS "TBH",
UTC, 02-03, pp 52, URL : https://www.utc.fr/~farges/dess_tbh/02-03/Projets/vbpb/vbpb.html
- ISO
9000 en santé : bilan Accréditation et certification au
service biomédical,
Projet DESS "TBH", UTC, 2000, pp 30. Hervé MIGNARDOT,
Hervé DION
URL : https://www.utc.fr/~farges/dess_tbh/99-00/Projets/bilan_ce/bilan_ce.htm
Relative
aux textes
réglementaires
Voir les
procédures en Annexe
(partie : documents et
références) :
Procédure d’accueil et d’encadrement des stagiaires (Annexe
12). 
Procédure de réception et de mise en service des
équipements neufs (Annexe 7). 
Procédure de maintenance préventive et contrôle
qualité des équipements
biomédicaux (Annexe 8) .
Procédure de maintenance corrective des équipements
biomédicaux (Annexe 9). 
Relative aux Guides
-
Guide de
maintenance des dispositifs médicaux, obligations
et recommandations, pp :
26 conception
réalisation : DRASS Midi-Pyrénées
- mars 2005. (date de
consultation: 15/03/08)
URL :
http://midi-pyrenees.sante.gouv.fr/santehom/vsv/vigilanc/materio/maint_dm.htm
-
Guide
des dispositifs médicaux, concepts et réalités de
terrain, pp : 36, conception réalisation : DRASS
Midi-Pyrénées – septembre 2006. (date de
consultation: 15/03/08)
URL :
http://midi-pyrenees.sante.gouv.fr/santehom/vsv/vigilanc/materio/maint_dm.htm
-
Réglementation
maintenance et contrôle qualité des dispositifs
médicaux, Réunion IBMH du 15
février 2007. pp : 144.
Relative
aux sites Internet
URL : http://www.afnor.fr
ou http://sagaweb.afnor.fr
AAMB
: Association des Agents de Maintenance
Biomédicale (http://www.aamb.asso.fr) ;
AFIB
: Association Française des
Ingénieurs
Biomédicaux (http://www.afib.asso.fr);
ATD
: Association des Techniciens de Dialyse
(http://www.dialyse.asso.fr);
AFNOR :
Association Française de Normalisation (http://www.afnor.fr);
AGEPS
: Agence Générale des Equipements et
Produits de Santé ;
ACHA
: Achats Centraux
Hôteliers et Alimentaires ;
AP-HP
: Assistance Publique -
Hôpitaux de Paris ;
BPF
: Bonnes Pratiques
Fonctionnelles ;
BPO
: Bonnes Pratiques
Opérationnelles ;
BP
: Bonnes Pratiques ;
DESS
: Diplôme d’Etudes Supérieures
Spécialisées ;
DHOS :
Direction de l’Hospitalisation et de l’Organisation des Soins du
ministère de
la Santé Française (http://www.sante.gouv.fr);
DM
: Dispositif médical ;
DE :
Direction des Equipements ;
ECME
: Equipement de Contrôle, de Mesure et
d’Essai ;
GBPB
: Guide des Bonnes Pratiques
Biomédicales en Etablissement de Santé [1];
GMAO
: Gestion de la Maintenance Assistée par
Ordinateur ;
GESMAD :
Gestion du Matériel
Disponible (http://gesmad.aphp.fr/);
CAMAD
: Commission
d'Attribution du Matériel Disponible
(http://www.aphp.fr/site/benevolat/camad.htm) ;
UTC
: Université de Technologique de
Compiègne (https://www.utc.fr) ;
SBM
: Service Biomédical ;
retour sommaire
-
Annexe
1 :
Organigramme d’organisation des services d’administration de
l’hôpital 
- Annexe
2 : Organigramme
d’organisation de la Direction des
Équipements 
- Annexe
3 : Enquête de
satisfaction 2007/2008 
-
Annexe
4 : Plan de la Direction des
Équipements 
-
Annexe
5
: Déclaration de
conformité 
-
Annexe 6
: Processus d’achat des petits et gros équipements
biomédicaux et
mobiliers 
-
Annexe
7
: Procédure de réception et de mise en service des
équipements biomédicaux
neufs 
Procés
Verbal de mise en service des équipements biomédicaux
neufs 
-
Annexe
8
: Procédure de maintenance préventive et/ou de
contrôle des équipements
biomédicaux 
-
Annexe 9
: Procédure de maintenance corrective des équipements
biomédicaux

-
Annexe
10
: Procédure de réforme des équipements
biomédicaux 
Fiche de
demande de défalcation des équipements
biomédicaux 
-
Annexe
11
: Procédure de pret et mise en expérimentation des
équipements
biomédicaux 
Fiche de
demande de mise en expérimentation
des équipements
biomédicaux

- Annexe
12 : Procédure d’accueil
et d’encadrement des
stagiaires 
Fiche de demande de
stage 
- Annexe 13 :
Manuel
Qualité 
- Annexe
14 : Tableau de
répartition des
délais d’intervention 



